HOME >> JVM NEWS 一覧 >> 個別記事
公益財団法人佐々木研究所は、2022年11月4日、がん細胞を七色に光らせて腹膜播種の仕組みを解明したことを発表した(参照:「プレスリリース」)。附属佐々木研究所の山口英樹副所長と宮崎允研究員を中心とした研究グループは、蛍光蛋白質を使ってがん細胞を七色に光らせることにより、進行した胃がん、卵巣がん、膵臓がん、大腸がんなどが起こす腹膜播種と呼ばれる転移の仕組みを明らかにした。
同研究は同法人附属杏雲堂病院、東京薬科大学、東京理科大学、国立がん研究センターとの共同研究で、文部科学省科学研究費補助金などの助成のもとに行われたもので、その研究成果は2022年10月28日に科学雑誌Cancer Lettersにオンライン掲載された。
- 「Tissue factor-induced fibrinogenesis mediates cancer cell clustering and multiclonal peritoneal metastasis」
- Makoto Miyazaki,Ayaka Nakabo,Yoshiko Nagano,Yuko Nagamura,Kazuyoshi Yanagihara,Rieko Ohki,Yoshikazu Nakamura,Kiyoko Fukami,Jun Kawamoto,Kenji Umayahara,Masaru Sakamoto,Keiichi Iwaya,and Hideki Yamaguchi
進行した胃がん、卵巣がん、膵臓がん、大腸がんなどは腹膜播種と呼ばれる転移を起こす。腹膜播種は、がん患者の生存率低下の大きな要因であるが、有効な治療法に乏しいのが現状で、機序解明と新しい治療法の開発が求められている。
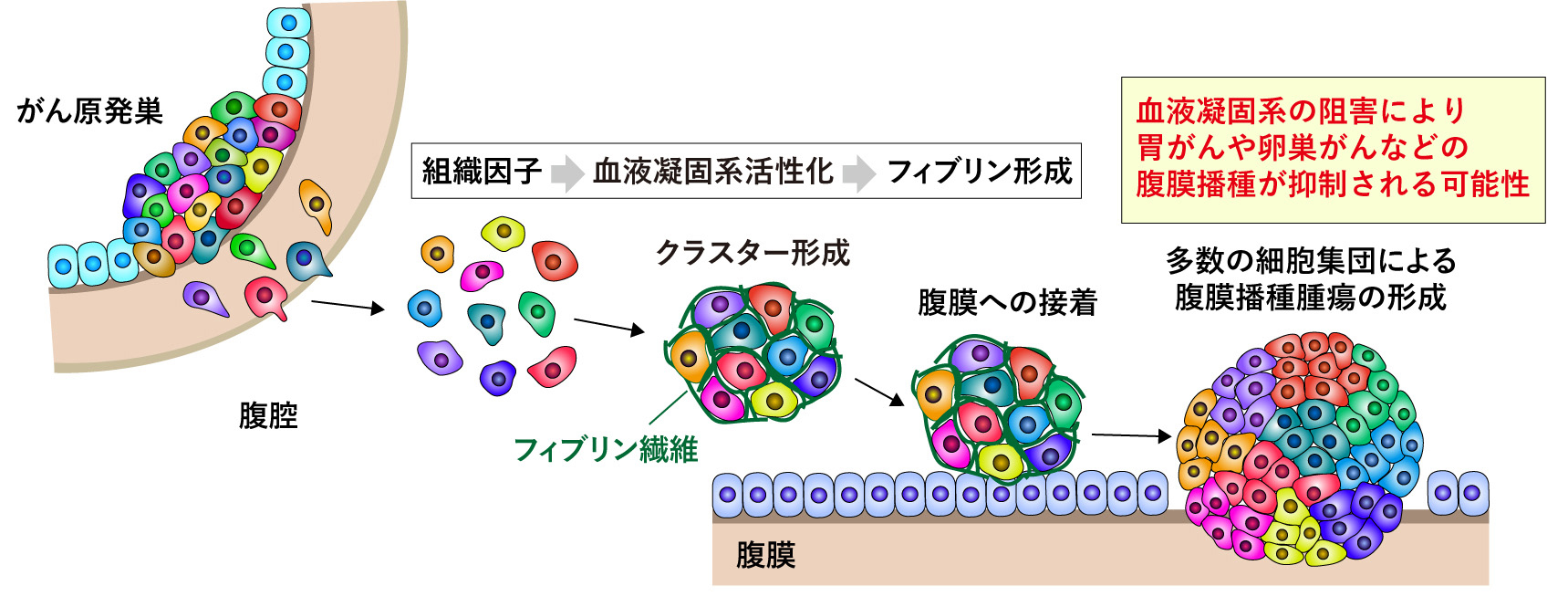
今回、研究チームはRGBマーキングという手法を用いて七色に光るがん細胞を作製した。この細胞をマウスの腹腔内に移植して、腹膜播種により形成された腫瘍を観察した結果、それぞれの腫瘍は複数の蛍光色を呈し、複数のがん細胞集団から構成されることが分かった。また、がん細胞は腹腔内でクラスターを形成し、集団で腹膜に接着して転移することが明らかになった。さらに、がん細胞が発現する組織因子が腹腔内で血液凝固系を活性化してフィブリンの形成を誘導すること、このフィブリンが糊のように働きがん細胞同士をくっつけて、腹膜への接着を助けることを発見した。実際にがん細胞の組織因子をノックアウトしてマウスに移植すると、フィブリンによるクラスター形成と腹膜播種が抑制された。したがって、がん細胞は組織因子により血液凝固系を活性化してフィブリン形成を誘導、腹腔内でクラスターを形成して集団で腹膜に接着することにより、多数の細胞集団から成るマルチクローナルな腫瘍を形成することが明らかになった。
同研究は、腹膜播種の腫瘍が複数のがん細胞集団により形成されること、その過程には血液凝固系の活性化やフィブリン形成が重要であることを初めて明らかにしたものであり、今後腹膜播種に対する分子標的治療法の開発に大きく貢献すると考えられる。
また同研究により、血栓症の治療などに使われている抗凝固薬が腹膜播種の治療薬や予防薬となる可能性が示された。